Alors que le focus se porte sur le microbiote intestinal dans bon nombre d’études scientifiques, le microbiote buccal requiert tout autant d’attention.
Le microbiote buccal peut se définir comme l’ensemble des micro-organismes présents dans la cavité buccale. Ces micro-organismes se constituent de centaines d’espèces de bactéries, qui cohabitent avec des virus, des fungi, des protozoaires et des archées.
Certains d’entre eux sont communs aux différents microbiotes de l’organisme, comme le Candida albicans, l’Helicobacter Pylori, la bactérie anaérobie Porphyromonas gingivalis, agent pathogène majeur de la parodontite. De la poche parodontale, ils migrent alors dans l’organisme via le système vasculaire.
D’autres sont spécifiques, comme les bactéries aérobies que nous respirons, ou anaérobies, difficiles à déloger des poches où elles se dissimulent.
C’est toute une population que notre bouche héberge et qu’il convient de maintenir en équilibre (eubiose), en favorisant les bactéries commensales, bénéfiques pour la santé. Cet équilibre écarte la colonisation par les agents pathogènes.
Lorsque le microbiote se retrouve en déséquilibre (dysbiose), les bactéries opportunistes prolifèrent et augmentent le risque d’infections locales. La flore devient pathogène.
Le microbiote buccal de chaque individu, très spécifique, pourrait se définir comme la carte d’identité de celui-ci. La flore buccale est influencée par les antécédents personnels et familiaux, par l’hygiène alimentaire, l’hygiène dentaire et buccale, l’hygiène de vie, l’état de santé et l’âge de celui-ci.
UNE HISTOIRE DE BIOFILM
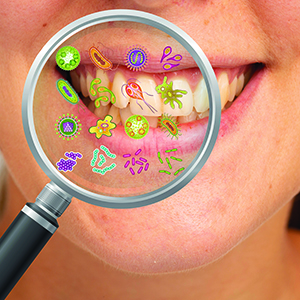
La cavité buccale est alors un écosystème très complexe. Les milliers de micro-organismes qui y sont hébergés, constituent une entité structurale spécifique : le biofilm buccal.
Ces micro-organismes, qui peuvent s’avérer pathogènes, adhèrent entre eux, se créant ainsi une matrice protectrice et adhésive et favorisant leur croissance.
Le biofilm, encore appelé « plaque bactérienne », se développe en milieu humide et la cavité buccale est une résidence de choix, où dents et implants deviennent des hôtes premium pour les bactéries. Au fur et à mesure, celles-ci s’agglutinent et forment un bouclier résistant, y compris aux antibiotiques, et difficile à éliminer. Le risque de caries et de maladies parodontales augmente.
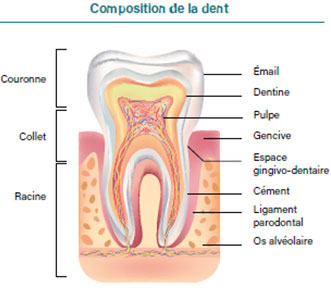
LA PARODONTITE
Les principales maladies parodontales sont la gingivite et la parodontite.
La première est une inflammation localisée, limitée à la gencive libre. La gencive gonfle, et saigne. En revanche elle n’entraîne pas la destruction des tissus de support sous-jacents. On peut alors constater un changement des populations bactériennes locales, avec une augmentation de certaines d’entre elles causée par l’accumulation de la plaque mais cette situation est réversible.
La parodontite, étymologiquement, renvoie à l’inflammation du parodonte. Sa caractéristique principale est d’atteindre le parodonte profond, c’est-à-dire l’os alvéolaire.
Le parodonte se compose de la gencive, de l’os alvéolaire, du ligament alvéodentaire et du cément.
La parodontite est une infection buccale à germes Gram négatifs. Elle se définit par la destruction de l’ensemble des tissus de support de la dent, et par conséquent l’os alvéolaire, le ligament parodontal et le cément.
Cette situation est la conséquence directe d’une infection causée par un groupe spécifique de bactéries et par la réponse immuno-destructrice de l’hôte. Dans ce cas, bien que l’évolution de la parodontite puisse être contrôlée, celle-ci se caractérise par son irréversibilité avec perte d’attache.
Plusieurs types de parodontites existent, progressives, virulentes ou chroniques. Celle-ci progresserait de façon cyclique et de manière corrélée à la réponse immunitaire plus ou moins efficace de l’individu.
BACTERIES ET FACTEURS DE VIRULENCE
Alors que les bactéries responsables de la gingivite appartiennent aux Streptococcus et Actinomyces, dans le cas de la parodontite, les bactéries à Gram négatif mises en évidence et retrouvées sur la plaque dentaire sont « Porphyromonas gingivalis », « Actinobacillus actinomycetemcomitans » et « Bacteroides forsythus ». Leur concentration et leur virulence créent l’infection parodontale. Elles franchissent les barrières de l’hôte, pouvant échapper au système de défense de celui-ci.
Un individu peut être infecté par « Actinobacillus actinomycetemcomitans » et n’exprimer aucun symptôme (douleur, plaque, tartre, ulcération). La bactérie peut alors coloniser des sites sous-gingivaux et créer des dommages tissulaires.
D’autres bactéries comme « Treponema denticola » ou encore « Campylobacter rectus » peuvent jouer un rôle dans le déclenchement de la parodontite cependant elles restent secondaires.
Il est important de souligner que les bactéries responsables des caries ne provoquent pas la perte d’attache rencontrée en cas de parodontite.
LES FACTEURS DE RISQUE
Contrairement aux idées reçues, l’âge n’est pas le premier facteur causal de la survenue de la parodontite. L’avancement dans l’âge de la population qui se voit

diagnostiquer une parodontite est le reflet du caractère progressif de la parodontite dans la destruction des tissus de support de la dent.
Parmi les facteurs de risque, les facteurs environnementaux :
Le tabagisme est désigné comme un facteur de risque important. La nicotine altère les fonctions des cellules phagocytaires, les « éboueurs de l’organisme », qui jouent un rôle essentiel contre les infections bactériennes.
Les déficits et les carences micronutritionnels constituent un facteur de risque important.
En effet des déficits et/ou carences en vitamines (C et D), oligo-éléments, minéraux, contribuent à déséquilibrer le terrain et participent au processus inflammatoire.
Dans ce contexte, certaines périodes de la vie d’un individu doivent être particulièrement suivies. Lors de la grossesse, de la ménopause, à la suite de certains traitements, ou de gros changements qui impactent l’équilibre quotidien.
Ceci nous amène à l’alimentation qu’il est nécessaire d’équilibrer en mettant en lumière non seulement les déficits et les carences qui nuisent à l’eubiose, mais aussi les excès qui participent au déséquilibre, entraînant la dysbiose.
Notre alimentation occidentale industrielle s’enrichit de sucres et de sels cachés. Elle est transformée et appauvrie, et ne nous apporte plus les micronutriments nécessaires pour être et rester en santé.
Le premier excès auquel nous pensons est le sucre, qui participe à l’apparition des caries, et qui contribue aussi à l’acidification du terrain.
Je citerai également les protéines, entre autres sources essentielles d’acides aminés pour le développement de la matrice osseuse. Quand elles sont en excès, elles déséquilibrent les microbiotes buccal et intestinal, et jouent un rôle dans l’acidose métabolique latente.
L’acidose métabolique entraîne des pertes minérales importantes au niveau rénal, et initie voire accentue des déficits déjà existants.
L’acidose chronique consiste en un processus intéressant à considérer dans la parodontite. Naturellement, notre métabolisme produit des déchets acides, et nous pouvons constater que l’alimentation occidentale contemporaine est plus acidifiante qu’alcalinisante.
L’équilibre entre les acides et les bases s’avère essentiel. En effet, les acides en excès s’accumulent dans le tissu conjonctif, et un phénomène inflammatoire de bas grade va se chroniciser sur un terrain acidifié. L’inflammation devient systémique, le système immunitaire est fragilisé, ouvrant la porte aux infections et diverses agressions, aux maladies.
ET LE STRESS DANS TOUT CELA ?

Une étude russe pointait le rôle du stress dans la perturbation du processus d’inhibition de la peroxydation lipidique. Celui-ci entraîne une baisse de la protection antioxydante des tissus mous du parodonte et initie ainsi le processus de la parodontite. Ce mécanisme de peroxydation provoque la destruction du collagène et la résorption osseuse.
Récemment, Zhang et Al. décrivent comment le stress psychologique accentue le développement de la parodontite. Il favorise la croissance bactérienne pathogène et l’expression des facteurs de virulence.
Le stress mental induit un dysfonctionnement endothélial, via, entre autres, la libération de cytokines pro-inflammatoires et apparaît alors comme un facteur de risque de l’inflammation systémique et chronique.
Inversement, le rôle du microbiote buccal sur la santé émotionnelle et psychologique est indéniable.
La production de cytokines pro-inflammatoires entraîne l’augmentation des niveaux de neuroinflammation par les voies humorales, neuronales et cellulaires.
FOCUS SUR L’INFLAMMATION
Le principal facteur de risque est la réponse inflammatoire et immunitaire médiée par l'hôte à l'accumulation de plaque microbienne ainsi que des facteurs génétiques et épigénétiques.
En effet la présence seule de bactéries pathogènes favorables au déclenchement de la parodontite ne suffit pas. C’est la réponse immunitaire de l’hôte en réponse à l’agression bactérienne qui va induire l’évolution de la parodontite. Certaines cytokines comme l’Il-1β, l’Il6, l’Il-8, le TNF-α favorisent le mécanisme inflammatoire par l’augmentation de la production de médiateurs de l’inflammation tels que la prostaglandine E2 (PGE2) provoquant des dommages tissulaires importants. Ils induisent le processus enzymatique qui s’ensuit par la production des MMPs, qui contribue elle-aussi à la destruction du collagène et à la résorption osseuse.
La conséquence directe de cette inflammation est la destruction du système d’attache parodontal.
IMMUNITE ET PARODONTITE
Par ailleurs, le rôle de certains virus comme l’Epstein Barr Virus, le CytoMegaloVirus, l’Herpes simplex attire toute l’attention aujourd’hui. Ils favoriseraient les co-infections bactériennes. Une étude de Contreras & Al, 1999, met en évidence une co-infection avec P. gingivalis en présence du virus Epstein Barr ou du CytoMegaloVirus.
Elle pointe également leur rôle dans la diminution de l’activité des cellules immunitaires en favorisant l’adhérence des parodontopathogènes sur les cellules infectées par les virus.
MALADIES DE SYSTEME…
Certaines situations de santé ou maladies systémiques peuvent prédisposer ou aggraver la parodontite. Selon l’Organisation Mondiale de la Santé, la parodontite touche 19 % de la population mondiale. Celle-ci pointe le lien de réciprocité entre le diabète de type 2 et l’apparition et l’évolution de la parodontite. Le facteur de risque pour les patients diabétiques serait de 2,5 à 4 fois plus élevé que celui d’un patient non diabétique. Leur situation parodontale est aggravée avec une poche parodontale plus profonde de 0,61 mm et une perte d’attache plus importante de 0,89 mm.
En effet, l’hyperglycémie prolongée provoque l’inflammation systémique chronique, diminue le pH et favorise la prolifération bactérienne au niveau de la plaque sous-gingivale. Il en découle une modification de la composition du microbiote oral. Elle altère le processus de réparation osseuse et fabrique des produits finaux de glycation avancée (AGE).
Dans le même temps, alors que de nombreux patients atteints de maladies cardiovasculaires ne présentent aucun des facteurs de risque traditionnels, certaines études identifient la parodontite comme un facteur de risque potentiel de l’athérosclérose.
En effet, lors de certaines manipulations médicales ou d’un simple brossage de dents, lors de la mastication, des bactéries buccales passent vers la paroi vasculaire par la circulation. Elles contribuent ainsi à la formation et au développement de la plaque d’athérome.
Par ailleurs, la parodontite provoque une augmentation des cytokines pro-inflammatoires au niveau du parodonte, et qui entrent dans la circulation. Ces mêmes cytokines circulantes sont identifiées comme des marqueurs des maladies cardiovasculaires ischémiques.
…ET INVERSEMENT
Inversement, la parodontite se révèle être un terrain favorable au développement de maladies de système, via des facteurs de risque partagés, tels que l'hébergement d'anaérobies pathogènes à Gram négatif dans les biofilms sous-gingivaux et la transformation du parodonte en réservoir de médiateurs pro-inflammatoires. Elle est associée aux problèmes cardiovasculaires, à l’athérosclérose, aux accidents cérébraux vasculaires, aux troubles thyroïdiens, aux abcès pulmonaires, au diabète, aux maladies auto-immunes, au risque de cancer, y compris à certaines naissances prématurées.
Toujours selon l’OMS, la parodontite sévère augmente l’incidence du diabète de type 2 de 53 %.
Par ailleurs, lorsque la thyroïde commence à dysfonctionner, des troubles thyroïdiens apparaissent, dont les plus fréquents sont l’hypothyroïdie et l’hyperthyroïdie.
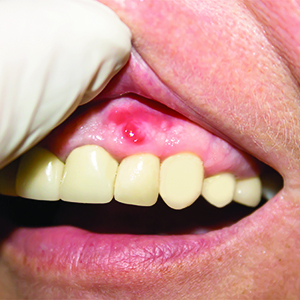 À ce moment-là, de nombreux changements physiologiques surviennent, y compris au niveau bucco-dentaire. On peut observer une hypoplasie de l'émail, une inflammation des tissus parodontaux et une perte osseuse alvéolaire.
À ce moment-là, de nombreux changements physiologiques surviennent, y compris au niveau bucco-dentaire. On peut observer une hypoplasie de l'émail, une inflammation des tissus parodontaux et une perte osseuse alvéolaire.
Le mécanisme de perte osseuse due à l’hypothyroïdisme dépend de plusieurs facteurs. Les équilibres biologiques sont bouleversés avec une augmentation du TNF-α et de l'IL-6. Par ailleurs, une densité osseuse plus faible existe également.
Dans le cas du cancer, les recherches actuelles s’orientent sur une corrélation entre parodontite et cancer.
Différentes études mettent en évidence le lien entre le microbiote oral, la parodontie et le risque de cancer. Les personnes connaissant une parodontite sévère auraient 24 % de risque supplémentaire de déclencher un cancer dans les 15 années à venir.
L’étude de Michaux & Al., 2018, met en évidence un risque élevé de cancer du poumon et de cancer colorectal chez les personnes souffrant de parodontite. Komlos & Al. étudient l’impact de la parodontite sur le cancer de la bouche. L'incidence du cancer de la bouche est de 57,1 % chez les patients atteints de maladie parodontale versus 28,6 % parmi les patients sans parodontite. La plupart des patients atteints d'un cancer de la bouche (72,1 %) souffraient d'une parodontite de stade 4. Bien évidemment les facteurs de risque génétiques, socio-économiques et d’hygiène de vie sont à considérer.
Les Maladies Inflammatoires Chroniques de l’Intestin (MICI) désignent une inflammation chronique non contagieuse de la paroi intestinale et résultant d’une réaction immunitaire et inflammatoire exacerbée à des antigènes bactériens normalement présents dans l’intestin.
Elles se caractérisent par la présence d’inflammation, ainsi que par la destruction de la barrière épithéliale.
Elles évoluent par poussées inflammatoires de durées variables (phase symptomatique) entrecoupées par des phases de rémission (phase asymptomatique).
Aujourd’hui encore, l’étiologie des MICI reste inconnue et on s’accorde à dire que leur origine est polyfactorielle.
Dans des proportions variables, des facteurs génétiques, environnementaux et un rôle du microbiote intestinal seraient impliqués dans la survenue de ces pathologies.
L’hypothèse étiologique actuelle décrit ces pathologies comme des réponses inflammatoire et immunitaire anormales vis-à-vis de la microflore intestinale, déclenchée ou aggravée par des facteurs environnementaux, chez des individus génétiquement prédisposés.
En plus des facteurs génétiques et environnementaux, de plus en plus d’arguments associent les MICI à une diminution de la biodiversité du microbiote intestinal et à son déséquilibre (dysbiose).
Or, les dernières études pointent le rôle du déséquilibre bactérien oral sur l’intestin. Bien que les mécanismes ne soient pas clairement identifiés, la parodontite est associée aux MICI (Elle & Al., 2020).
Les patients atteints de MICI présentent alors un déséquilibre du microbiote oral, des bactéries commensales orales à pathogénicité opportuniste étant retrouvées en surnombre dans le microbiote intestinal des patients atteints de MICI.
Ces bactéries buccales participent à la destruction de la barrière épithéliale intestinale, provoquent une sécrétion excessive de cytokines inflammatoires et entraînent une perturbation du système immunitaire de l'hôte. La dysbiose intestinale aggrave l’inflammation intestinale chronique.
La polyarthrite rhumatoïde est également une maladie auto-immune chronique caractérisée par une inflammation synoviale pouvant entraîner des lésions du cartilage articulaire et des os. Le lien entre la polyarthrite rhumatoïde et la dysbiose intestinale et buccale est établi, ainsi que la corrélation à long terme entre la maladie parodontale et la polyarthrite rhumatoïde. Lors de la prise en charge de la polyarthrite rhumatoïde, l’eubiose de la cavité buccale est en partie retrouvée.
QUELLES SONT LES SOLUTIONS
Continuer d’éduquer en matière d’alimentation
L’appauvrissement des sols, l’alimentation des troupeaux, la transformation industrielle des aliments et les modes de cuisson ont modifié de manière significative notre alimentation. Les aliments contiendraient moins de nutriments qu’avant. Les études sur le sujet indiquent que la concentration de certains nutriments importants tend à baisser. Des travaux menés aux États-Unis sur 43 fruits et légumes, ainsi que sur des céréales, et publiés en 2004, indiquent que les concentrations ont baissé de 20 % pour la vitamine C. D'autres aliments voient eur statut micronutritionnel également diminuer : 15% pour le fer (blettes, concombre, feuilles de navet), 16 % pour le calcium (choux kale, brocolis...)ou encore 6 % pour les protéines (Donald Davis, chercheur à l’Institut biochimique de l’université du Texas).
Selon nos choix alimentaires et nos modes de consommation, les apports en micronutriments, la charge glycémique, la composition en acides gras, la teneur en minéraux, la teneur en fibres d’un repas et le pH alimentaire seront optimaux ou non. Aujourd’hui il est essentiel de poursuivre l’éducation alimentaire des personnes que nous rencontrons en consultation en les alertant sur les sels et sucres cachés, sur l’alimentation raffinée et transformée, sur une alimentation très riche en céréales et pauvre en légumes et fruits, trop riche en certaines protéines et en leur expliquant les dangers de tels choix alimentaires sur leur santé bucco-dentaire et par conséquent sur leur santé tout simplement.
Ceci est d’autant plus important dans le contexte économique actuel qui pose question sur le contenu de l’assiette avec une inflation galopante qui touche l’alimentation soit 11,1 % d’augmentation des prix alimentaires sur un an en août 2023, 18 % sur les dix-huit derniers mois. Dans le détail, le prix du panier de fruits a augmenté de 14 % en conventionnel et de 8 % en bio, celui du panier de légumes de 17 % en conventionnel et 15 % en bio.
Rééduquer les gens à la mastication
La mastication accrue semble efficace pour aider à interrompre la formation de plaque en abrasant mécaniquement les surfaces dento-gingivales. Dutzan et al. ont démontré que la texture et la dureté d’un aliment modifient le microbiote oral et la réponse immunitaire au niveau de la gencive, en induisant mécaniquement la production de cellules T-helper 17, et en dressant une barrière de protection au niveau de la gencive.
Par ailleurs, la mastication stimule les glandes salivaires pour produire de la salive. La salive joue un rôle essentiel dans le maintien de la santé bucco-dentaire et dans la régulation du microbiote buccal sain. Elle fournit une pellicule à l'émail et à la muqueuse acquise qui représente la base de la colonisation initiale des tissus durs et mous par les micro-organismes. Elle contient des substances telles que le lysozyme qui, comme le mucus, protège la muqueuse digestive, et a une action bactéricide en inhibant la croissance bactérienne.
Se réconcilier avec l’hygiène dentaire
« Le brossage des dents déplace mécaniquement les bactéries buccales et la plaque dentaire de la dentition et de la gencive afin de limiter les dommages à long terme causés par leurs sous-produits métaboliques » salon l'American Dental Association.
Se brosser les dents avec une brosse à dents souple deux à trois fois par jour, durant 2 à 3 minutes est essentiel. Comme il apparaît essentiel de remplacer celle-ci tous les trois à quatre mois car la brosse à dents est exposée aux microbes de la bouche, à l'environnement, aux mains…
Par ailleurs, des dentifrices ont été formulés pour rééquilibrer l’écosystème buccal. Certains contiennent des protéines conçues pour favoriser la santé bucco-dentaire. Il est simple de demander conseil à son dentiste.
Différentes études mettent en avant l’intérêt de l’utilisation du miswak, obtenu à partir de la racine de Salvadora persica, une plante utilisée comme brosse à dents naturelle depuis l’Antiquité. Il est utilisé en Asie, en Inde, et bien évidemment dans les Pays d’Afrique et du Proche Orient. Les conclusions l’imposent comme réduisant les scores de plaques dentaires. Son utilisation complémentaire à la brosse dents s’avère efficace pour lutter contre les maladies parodontales.
Les probiotiques
Enfin, l'impact positif de la consommation de probiotiques sur la santé gastro-intestinale est bien documenté. Aujourd’hui, leur rôle dans l’eubiose des autres microbiomes est regardé de très près et les derniers essais cliniques chez l'homme démontrent que les probiotiques ont le potentiel de modifier la composition du microbiote sous-gingival, en abaissant considérablement la concentration des bactéries pathogènes.
La gélule de probiotiques peut également être ouverte et libérée directement dans la bouche, en maintenant son contenu en bouche pendant 3 minutes.
L’aloe vera
La plante d’Aloes est vénérée depuis l’Antiquité. Des tablettes d’argile datant de plus de 4000 ans témoignent de ses pouvoirs de guérison particuliers. Elle porte de nombreux surnoms, de « lys du désert » à « impératrice des plantes médicinales ». L'aloe vera (Aloe barbadensis) appartient à la famille des Liliacées.
L’aloe vera contient divers composants dotés de caractéristiques antibiotiques et anti-inflammatoires, qui peuvent présenter des avantages potentiels pour traiter les maladies parodontales. On lui confère un rôle cicatrisant et antiseptique. Par ailleurs, elle est riche en enzymes, et ses mucilages contribuent à l’amélioration du pH intestinal.

Gérer l’équilibre acido-basique
Par l’alimentation comme vu plus haut, l’hygiène de vie, la gestion du stress, l’activité physique et également, en apportant des citrates et des minéraux notamment, de manière ponctuelle et en cure, à minima pour appuyer la régulation et faciliter l’élimination des acides métaboliques.
L’ubiquinol (forme réduite et la plus active biologiquement de la coenzyme Q10)
Face à l’agression bactérienne et à la réponse immunitaire de l’hôte qui produisent des radicaux libres et des espèces réactives de l’oxygène (ROS), la coenzyme Q10 s’avère un antioxydant majeur. Il participe à freiner la dégradation du collagène et des cellules parodontales. Il permet de lutter contre l’inflammation parodontale.
La prise de coenzyme Q10 réduirait l’indice de la plaque, l’indice de saignement et la profondeur de la poche. Ses propriétés s’avèrent intéressantes en prévention comme en curatif.
L’arrêt du tabac
Afin de diminuer la pathogénicité du biofilm oral, l’arrêt total, à minima une diminution drastique du tabac est fortement conseillé. La diminution de la consommation d’alcool également quand celle-ci est en excès.
Rencontrer son dentiste
Une visite annuelle chez le dentiste pour un détartrage à minima est recommandée.
 |
Article rédigé par Delphine ROLAND Micronutritionniste, Naturopathe Médecine fonctionnelle et nutritionnelle |